熱力学の法則とは何か、これらの原理の起源は何か、そしてそれぞれの主な特徴について説明します。

熱力学の法則は何ですか?
熱力学の法則(または熱力学の法則)は、3つの基本的な物理量の振る舞いを説明しています。 温度、 エネルギー そしてそのエントロピ、熱力学系を特徴付ける。 「熱力学」という用語はギリシャ語に由来します 魔法瓶、 どういう意味ですか "熱"、Y ダイナモ、 どういう意味ですか "力”.
数学的には、これらの原則は次のように記述されます。 セットする 熱力学系の振る舞いを説明する方程式の例。 分子 または 人間、 それまで 雰囲気 または鍋で水を沸騰させます)。
熱力学の法則は4つあり、それらは熱力学の法則を理解するために重要です。 宇宙 とのような特定の現象の不可能性 動き パーペチュアル。
熱力学の法則の起源
の4つの原則 熱力学 それらは異なる起源を持っており、いくつかは以前のものから処方されました。実際、最初に設立されたのは、1824年にフランスの物理学者でエンジニアのニコラ・レオナルド・サディ・カルノーの作品でした。
しかし、1860年に、この原理はルドルフ・クラウジウスとウィリアム・トンプソンによって再び定式化され、現在、熱力学の第1法則と呼ばれているものが追加されました。その後、1906年から1912年にかけてのヴァルター・ネルンストの研究のおかげで生じたため、「ネルンの仮説」としても知られる3番目の作品が登場しました。
最後に、いわゆる「ゼロ法則」が1930年に登場し、グッゲンハイムとファウラーによって提案されました。すべての分野でそれが真の法として認められているわけではないということは言われるべきです。
熱力学の第一法則

最初の法則は「エネルギー保存の法則」と呼ばれます。 システム 環境から隔離されているため、ある形式のエネルギーから別の形式のエネルギーに変換できる場合でも、エネルギーの総量は常に同じになります。言い換えれば、エネルギーは生成または破壊することはできず、変換されるだけです。
したがって、与えられた量の熱(Q)を物理システムに供給することにより、その総エネルギー量は、供給された熱から仕事 (W)システムがその周囲で実行します。式で表されます:ΔU= Q-W。
この法則の例として、飛行機のエンジンを想像してみましょう。これは、燃料のプロセス中に化学的に反応する燃料で構成される熱力学システムです。 燃焼、熱を放出して機能します(飛行機を動かします)。つまり、行われた仕事の量と放出された熱を測定できれば、システムの総エネルギーを計算し、飛行中のエンジンのエネルギーは一定であると結論付けることができます。エネルギーは生成も破壊もされておらず、変更されました。の 化学エネルギー に カロリーエネルギー Y運動エネルギー (動き、つまり仕事)。
熱力学の第二法則
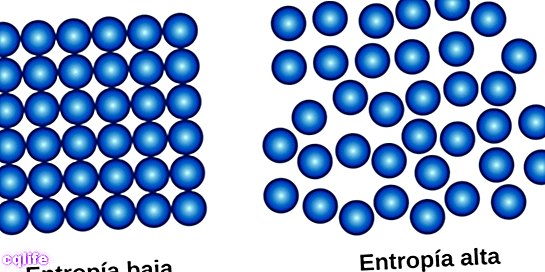
«エントロピーの法則»とも呼ばれる第2の法則は、次のように要約できます。 エントロピ 宇宙では増加する傾向があります 天気。これは、システムの無秩序の程度が、システムの最大の無秩序の状態である平衡点に達するまで増加することを意味します。
この法則は、物理学の基本的な概念を導入しています。エントロピーの概念(文字Sで表されます)は、物理システムの場合、無秩序の程度を表します。エネルギーの変換があるすべての物理的プロセスでは、一定量のエネルギーが使用できない、つまり仕事ができないことがわかります。あなたが仕事をすることができないならば、ほとんどの場合、そのエネルギーは熱です。システムが放出するその熱、それがすることは、システムの無秩序、そのエントロピーを増加させることです。エントロピーは、システムの無秩序の尺度です。
この法則の定式化により、エントロピー(dS)の変化は常に熱伝達 (dQ)、システムの温度(T)で割った値。つまり、dS≥dQ/ Tです。
例を挙げてこれを理解するには、ある程度の量を燃やすだけで十分です 案件 次に、得られた灰を収集します。それらを計量するとき、それが初期状態にあったものよりも問題が少ないことを確認します:問題の一部は次の形で熱に変換されました ガス 彼らはシステムで仕事をすることができないこと、そして彼らはその無秩序に貢献していること。
熱力学の第三法則

第3法則は、絶対零度になるシステムのエントロピーは明確な定数になると述べています。言い換えると:
- 絶対零度(ケルビン単位でゼロ)に達すると、物理システムのプロセスが停止します。
- 絶対零度(ケルビン単位でゼロ)に達すると、エントロピーの最小値は一定になります。
日常的にいわゆる絶対零度(-273.15°C)に到達することは困難ですが、冷凍庫で何が起こっているかを分析することで、この法則について考えることができます。 食物 そこに堆積すると非常に冷たくなり、その中の生化学的プロセスが遅くなるか、停止することさえあります。そのため、分解が遅れ、 消費 ずっと長く。
熱力学のゼロ法則
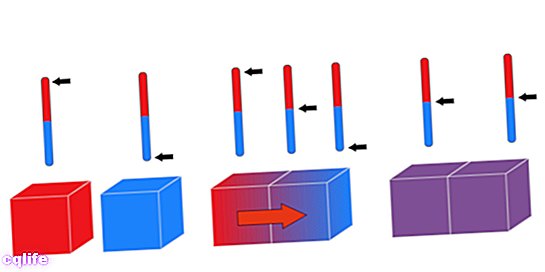
「熱力学第零法則」は、最後に実行されたものですが、その名前で知られています。としても知られている 熱平衡の法則、この原則は次のように指示します。 熱平衡 3番目のシステムとは独立して、それらも互いに熱平衡にある必要があります」。論理的には次のように表すことができます。A= CおよびB = Cの場合、A = Bです。
この法則により、3つの異なる物体A、B、およびCの熱エネルギーを比較できます。物体Aが物体Cと熱平衡にあり(同じ温度)、BもCと同じ温度である場合、AとBは同じ温度です。
この原理を述べる別の方法は、温度の異なる2つの物体が接触すると、温度が等しくなるまで熱を交換すると主張することです。
この法則の日常の例は簡単に見つかります。冷水または温水に入ると、体が熱平衡に入るため、最初の数分間だけ温度差に気付くでしょう。水 違いに気付くことはもうありません。暑い部屋や寒い部屋に入るときも同じことが起こります。最初は温度に気づきますが、熱平衡に入るため、違いの認識を停止します。
