蒸留とは何か、この分離方法の例、使用できる蒸留の種類について説明します。

蒸留とは何ですか?
蒸留は相分離の方法と呼ばれ、 混合物の分離方法。蒸留は、2つの物理的プロセスの連続的かつ制御された使用で構成されています。 気化 そしてその 結露、それらを選択的に使用して、 混合 通常、均質タイプ、つまり、そのコンポーネントを肉眼で区別できないタイプです。
蒸留を使用して個々の成分に分離できる混合物には、2つを含めることができます 液体、 個体 液体またはさらに ガス スムージー。この分離方法は、沸点の違いに基づいています( 案件、何ですか 温度 それに プレッシャー 液体の蒸気は、さまざまな物質の液体を取り巻く圧力に等しくなります。最も低い物質 沸点 持っていると、この物質は別の容器で凝縮し、比較的純粋になります。
このように、蒸留が正しく行われるためには、混合物がいずれかの沸点に達するまで混合物を沸騰させる必要があります。 物質 成分は蒸気になり、冷却された容器に導かれ、そこで凝縮して再び液体になります。
一方、他の構成物質は、変更されることなくコンテナ内に残ります。しかし、どちらの場合も 純粋な物質、最初のミックスから解放されます。
ラウールの法則
液体の理想的な混合物( 粒子 異なるものは等しい粒子間の相互作用に等しいと見なされます)ラウールの法則が満たされます。
この法則は、ガス混合物中の各成分の部分蒸気圧は、純粋な成分の蒸気圧に液体混合物中のそのモル分率を掛けたものに等しいと述べています。
したがって、全蒸気圧は、気相中の混合物の成分の分圧の合計です。一方、混合物中の成分のモル分率は、その濃度の無次元の尺度です。上記のマグニチュードは、次の式を使用して計算できます。
どこ:
- px Y py コンポーネントの分圧です バツ と Y それぞれ、液体混合物を取り巻く蒸気の混合物。
- px *およびpy *は、コンポーネントの蒸気圧です。 バツ と Y。
- xx Y xy 成分のモル分率です バツ と Y 液体混合物中。
- nx Y ny 成分の物質量です バツ と Y 液体混合物中。
上で提起されたラウールの法則は、理想的な混合物(研究を単純化するために人間によって確立されたモデル)に有効ですが、実際には、混合物が実際の場合、この法則は逸脱します。
したがって、混合物中の異なる粒子が純粋な液体中の粒子よりも強い分子間力を持っている場合、混合物の蒸気圧は純粋な液体の蒸気圧よりも低く、Raoultによる法則からの負の偏差が生じます。
一方、純粋な液体中の粒子間の分子間力が混合物中の粒子の分子間力よりも大きい場合、混合物中の粒子はより容易に気相に逃げることができるので、蒸気圧は混合物の割合が大きくなり、ラウールの法則から正の偏差が生じます
共沸混合物(エタノールと水など)を蒸留する場合は、共沸混合物を変更して、このようにして共沸混合物の成分を分離できるように、いくつかの成分(この場合はベンゼン)を追加する必要があります。混合。共沸混合物は、沸騰したときに生成される蒸気が混合物の同じ組成を有する、定義された組成を有する液体混合物である(したがって、共沸混合物の成分は、単純または分別蒸留によって分離することはできない)。
共沸混合物の沸点は定義されており、たとえば、圧力1 atmで、エタノールは78.37°Cで沸騰し、水は100°Cで沸騰しますが、エタノール-水共沸混合物は78.2°Cで沸騰します。共沸混合物は、場合によってはラウールの法則から負または正の偏差があります。
蒸留の種類
蒸留はさまざまな方法で発生する可能性があります。
- 簡単な蒸留。最も基本的なことは、異なる成分が分離されるまで混合物を沸騰させることです。混合物の成分の沸点が大きく異なる場合に効果的な分離方法です(理想的には、少なくとも25°Cの差がある必要があります。そうでない場合、蒸留物質の全純度が保証されません)。
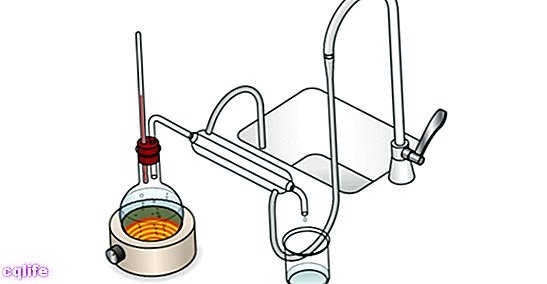
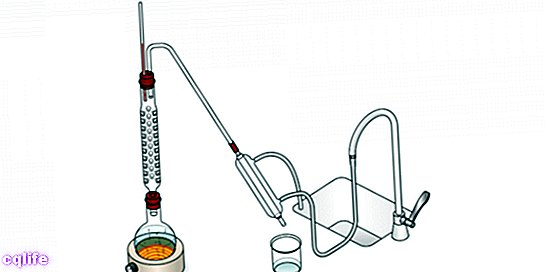
- 分別蒸留。それは、気化と凝縮が連続して行われる異なるプレートで構成されている分留塔によって実行され、分離された成分のより高い純度を保証します。
- 真空蒸留。真空が発生するまで圧力を下げることにより、プロセスが触媒されて成分の沸点が低下します。これは、圧力が大幅に低下したときに低下して蒸留プロセスを加速できる非常に高い沸点を持つものがあるためです。
- 共沸蒸留。共沸混合物、つまり、物質が1つとして振る舞い、沸点を共有している混合物を分解するために必要な蒸留であるため、単純な蒸留や分別蒸留では分離できません。共沸混合物を分離するには、例えば、いくつかの分離成分を加えることによって、混合条件を変更する必要がある。
- 水蒸気蒸留。混合物の揮発性成分と非揮発性成分は、水蒸気の直接注入によって分離されます。
- 乾留。それは、存在せずに固体材料を加熱することで構成されています 溶剤 液体、ガスを取得し、別の容器に凝縮します。
- 改善された蒸留。代替蒸留または反応蒸留とも呼ばれ、分離が困難な混合物や同じ沸点を持つ混合物の特定の場合に適合します。
蒸留の例

- 石油精製。さまざまなの分離 炭化水素 に存在する 石油 それは、原油の調理から得られた各化合物を蒸留塔の異なる層または別々の区画に貯蔵する分別蒸留によって実施されます。これらのガスはカラムの上層で上昇して凝縮しますが、アスファルトやパラフィンなどのより密度の高い物質は下層に残ります。
- 接触分解。これは、原油調理からガスを分離するために真空塔を使用する、石油処理における特定の通常の真空蒸留に付けられた名前です。したがって、炭化水素の沸騰が加速され、 処理する。クラッキングは破壊的蒸留の一種であり、大きな炭化水素が(高温で触媒を使用して)より小さな炭化水素に分解され、沸点が低くなります。
- エタノール精製。分離するために アルコール 実験室での製造中の水からのエタノールのように、共沸蒸留が使用され、混合物にベンゼンまたは分離を促進または加速する他の成分を追加し、その後、化学組成を変えることなく簡単に除去することができます 製品.
- 石炭処理。液体有機燃料を得るために、石炭または木材が乾留手順によって使用されるため、 燃焼.
- ミネラル塩の熱分解。乾留により、ミネラル塩を燃焼させて得られるガスの発生と凝縮から、工業的有用性の高い様々なミネラル物質が得られます。
- アレムビック。これはアラブの古代で発明された装置に付けられた名前であり、その目的は発酵した果物から香水、薬、アルコールを生産することです。その操作では、蒸留の原理が使用されます。物質は小さなボイラーで加熱され、生成されたガスはコイルで冷却され、別の容器に導かれ、そこでガスの凝縮によって生成された液体が収集されます。
- 香水の生産。水蒸気蒸留を使用して香水を取得し、保存された花と一緒に水を沸騰させて、目的の香りのガスを生成します。このガスは、凝縮すると、香水のベース液として使用できます。


